医学科普
发表者:李建辉 人已读

目前,中国不孕不育患者已超4000万,成为一个不容忽视的问题,这一问题可占育龄夫妇的15%。其中,男性因素约占50%,大多数患者无法获得明确的病因诊断。

在这些患者之中,约有30%的患者由遗传学因素导致。如果这部分患者没有通过遗传学检查明确诊断,可能会继续尝试性用药或手术治疗,从而延误病情、浪费医疗费用。
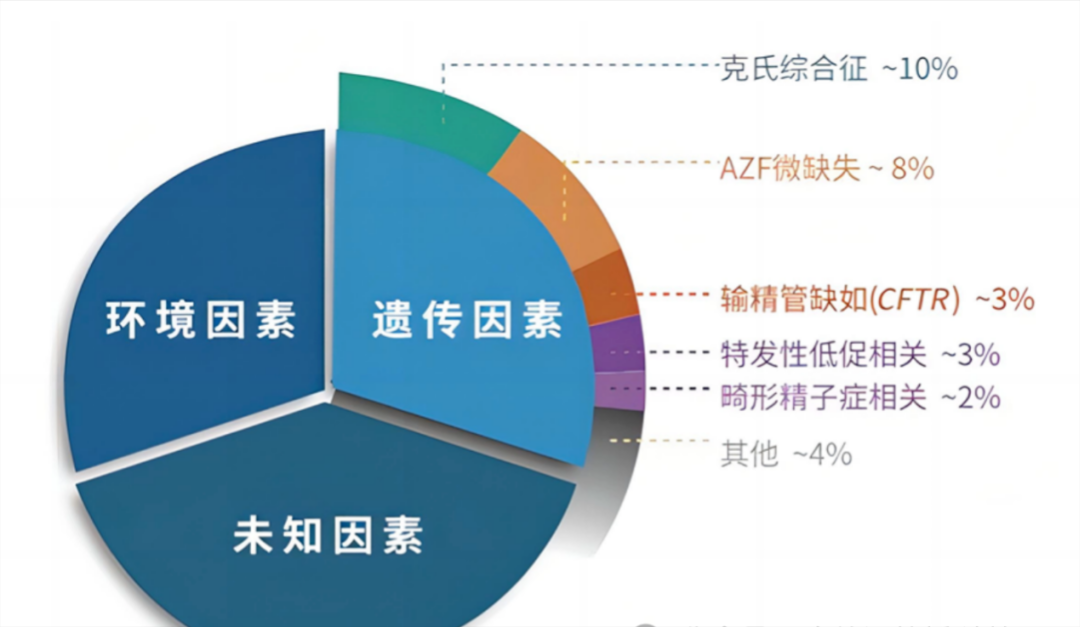
精子生成相关的基因缺失、突变或表达异常,都可能导致精子生成障碍,形成少精子症、弱精子症或无精子症,最终导致男性不育。

精子的发生是一个受到精细调节的众多基因共同参与的复杂而有序的过程。男性不育症患者是否需要做基因检测,应该做哪些基因检测呢?
一.什么是基因检测?
基因,它们是人体内那些神奇的密码,掌控着我们的身高体重、皮肤颜色,甚至影响我们的美丽与丑陋。当这些基因发生致病的变异时,它们就像电脑程序中的bug,可能导致各种遗传性疾病,例如:输精管缺如、畸形精子症、少弱精等。这些疾病就像人生的绊脚石,阻碍着我们追求当爸爸步伐。
而当这些基因发生变化影响到生育功能时,就像种子无法在贫瘠的土地中生长一样,会导致不孕不育。基因检测就像使用翻译软件的翻译官,它能帮助我们识别出基因中的变异,为医生提供治疗疾病的线索和参考。
通过基因检测,我们可以更好地了解自己的身体,预防和治疗一些遗传性疾病,从而让我们的生活更加健康、美好。基因检测就像为我们打开了一扇通向未来的门,让我们能够更好地掌控自己的生命。
二.什么是“生育基因检测”?
打个比方,把人体发育比喻成 “盖楼房”,基因则是一本蓝图,而蛋白质、糖、微量元素等等则是砖瓦、水泥、钢筋。基因出现变异,是蓝图出现错误,属于“先天” 问题。而 “施工过程” 出现的问题则属于后天问题。

不孕不育可以是 “蓝图” 问题,也可以是 “施工” 问题。例如,遗传物质产生改变,属于先天问题;而抽烟、喝酒、接触污染等环境问题属于后天问题。对于后天问题,相对来说容易改善;而对于先天问题,目前较难改善,大多只能通过辅助生殖技术完成生育。
不孕不育已证明和特定的基因有关系,目前已经发现超过100个基因和男性不育相关。基因检测可以检查与生育功能有关的基因是否发生了 “突变”。
三.男性不育为什么要做基因检测呢?
从本质上讲,基因变异导致的不孕不育也是一种遗传病,致使患者生育功能受损,不能自然生育后代。近些年,随着医学诊断技术的发展,科学家对这些基因变异的理解越来越深入,发现遗传变异是造成不孕不育非常重要的病因之一。据统计,男性不育中遗传因素占比高达30-35%。通过基因检测能够明确是否存在已知致病基因变异,其中部分已知致病基因变异已有较好的临床预后手段,这对于后续的治疗尤为重要。
四.测了有什么用?
1、明确发病原因,减少尝试性治疗:
很多患者经过1年、2年,甚至长达10多年的治疗,还是不能生育。非常希望搞清楚导致自身不育的原因到底是什么。通过基因检测,明确是否是遗传的原因,从而选择合适的治疗方案,减少尝试性治疗和过度治疗。
2、评估药物治疗是否有效果:
如:畸形精子在、弱精子症患者,通过基因检测,评估是否是基因突变造成的,如果是,临床再评估是否继续药物治疗及后续辅助生殖方案。
3、显微手术取精前,预判是否能够取到精子:
《男性生殖相关基因检测专家共识》指出,推荐对NOA(非梗阻性无精子症)患者在手术取精前,使用NGS(高通量测序技术)对无精子症相关致病基因进行检测。如:Tex11基因变异导致的无精子症,临床上通过手术获得精子的成功率较低,及时告知患者风险,减少患者的手术伤害及经济损失。
4、遗传阻断,指导优生优育:
部分遗传原因致病的不育患者,有可能将致病基因传递给下一代,导致下一代不育,甚至有罹患其他的疾病风险,这类患者需重视遗传咨询。如:CFTR基因变异导致的输精管缺如患者,若配偶同样携带CFTR致病变异,后代有不育的风险,甚至有囊性纤维化的风险,严重的会影响生命。
5、辅助判断辅助生殖技术治疗预后
如:基因突变也会导致精子的畸形,有头部畸形、尾部畸形等,相关文献报道,不同基因导致的畸形精子症,辅助生殖技术治疗预后不一样。如:DNAH1基因突变导致的畸形精子症患者,治疗预后结局良好;DNAH17基因突变的患者治疗预后结局不好。
6、风险提示,其他身体健康疾病管理:
男性不育相关基因,除了导致不育之外,还有可能伴有其他的系统异常,明确诊断是否基因突变导致的,有利于自身健康管理。如PKD1基因变异,除导致男性少精子症、无精子症之外,还与多囊肾发生相关。
五.对于男性因素不育的男性,
建议进行哪些基因检查?
对于无精子症、严重少精子症或者特殊精液状态的患者,我们通常会要求患者进行详细的基因检测分析。
患者听到“基因检测”四个字之后的第一反应就是 —— 陈医生,这个染色体我们做过的!
染色体三个字,基因检测四个字,为什么非要混为一谈啊!我们一直会告诫患者及其家属,请不要用你对疾病的认知,来衡量医生对疾病的专业度!
还有患者会说,基因检测,不就是做过“Y染色体微缺失”嘛,我们都做过的!
遗传学评估里面,包括了:染色体核型分析、Y染色体微缺失等常规检查以及基因突变检测等特殊检查。
01
核型(也称为染色体分析)
该测试检查染色体的数量和``设置‘‘,并可以检测一个人是否缺失或拥有整个染色体的额外副本,或很大一部分遗传密码。
02
Y染色体微缺失测试
Y染色体长臂上存在控制精子发生的基因,称为无精子因子(azoospermia factor,AZF);1996年Vogot等将AZF分为AZFa、AZFb、AZFc3个区域,1999年Kent等认为在AZFb区与c区之间还存在AZFd区。AZF的缺失或突变可能导致精子发生障碍,引起少精子症或无精子症。Y染色体微缺失目前主要是指AZF缺失,研究认为,在无精子症和少精子症的患者中,AZF缺失者约占3%~29%,发生率仅次于Klinefelter综合征,是居于第2位的遗传因素。目前,Y染色体微缺失的常用检测方法包括实时荧光定量PCR法、多重PCR-电泳法等。
03
基因突变检测
目前已知CFTR基因突变可引起囊性纤维化(CF;OMIM219700)和先天性双侧输精管缺如(CBAVD;OMIM 277180)。此外研究还发现它与慢性胰腺炎、睾丸生精功能障碍、精子受精功能障碍、女性生殖能力等多种疾病相关,甚至与肿瘤的发生、发展相关。已有研究发现存在CFTR基因突变的CBAVD患者ART时有更高的流产、死胎风险。因此,有必要针对上述患者进行特定基因突变筛查和遗传咨询,指导临床治疗。
基因测试的结果可以帮助您的生育专家了解在睾丸中找到精子的可能性。基因疾病专科的医疗保健提供者还可以向人们提供他们的基因检测结果,并建议他们是否可能将遗传异常传给未来的孩子。
六.测哪些基因?
对哪些基因进行检测,需要根据患者的临床表现来判断。临床表现可大致分为性发育异常(如睾丸体积偏小、男性化不足等)、无精子症、少/弱/畸形精子症三类,每一类中均可进一步细分。需要根据不同的表型类别,初步判断临床表现和哪些基因相关,从而选择这些基因进行测序。

1.生精障碍65型

根据ACMG指南,
DNHD1:NM_144666.3:c.522_525delGCAG(p.Arg174Serfs*3)为致病ACMG证据:PM2_Supporting,PVS1,PM3PM2_Supporting:gnomAD数据库中正常对照人群中未发现的变异(或隐性遗传病中极低频位点)。
PVS1:当一个疾病的致病机制为功能丧失(LOF)时,检出变异为无功能变异(无义突变、移码突变、经典±1或2的剪接突变、起始密码子变异、单个或多个外显子缺失)。
PM3:在隐性遗传病中,在反式位置上检测到致病或疑似致病变异。
▶DNHD1基因与生精障碍65型(OMIM:619712)疾病相关,为常染色体隐性遗传(AR),理论上1对常染色体上的等位基因发生致病变异可导致疾病的发生。
▶本次检测出DNHD1基因的变异,变异位点为c.522_525delGCAG(p.Arg174Serfs*3),为移码变异。该变异最高人群频率0.000032。该变异在ClinVar数据库收录为致病变异,星级1星。
据文献报道,该变异在1例弱精症患者中检出复合杂合携带。依据ACMG标准,判定该变异的致病性为致病。具体情况请结合临床相关资料综合判断。(PMID:34932939)
生精障碍65型(Spermatogenicfailure65):
生精障碍65型是由无精子症引起的男性不育症。进行性精子活力严重降低或缺失,患者表现出鞭毛的多种形态学异常,包括盘绕、口径不规则、短而无鞭毛、鞭毛中段的异常。临床表现:常染色体隐性遗传,男性不育,精子浓度降低,进行性运动减少或缺乏,鞭毛的多种形态异常,卷曲鞭毛,不规则口径鞭毛,短鞭毛,无鞭毛,畸形中段肿胀
2.精子形成障碍39型

精子形成障碍39型(Spermatogenicfailure39):精子形成障碍39型是由于鞭毛(MMAF)的多种形态学异常而导致不育。临床表现:常染色体隐性遗传,少精症,男性不育,精子活力降低,精子鞭毛缺失,精子鞭毛短,精子鞭毛卷曲,锥形精子头。
3.脑白质营养不良和获得性小头畸形伴或不伴张力失调

脑白质营养不良和获得性小头畸形伴或不伴张力失调(Leukodystrophyandacquiredmicrocephalywithorwithoutdystonia):脑白质营养不良和获得性小头畸形伴或不伴张力失调是一种常染色体隐性遗传的神经系统疾病,其特征为极重度精神发育迟缓、肌张力失调、出生后的小头畸形和与脑白质营养不良一致的白质异常。临床表现:常染色体隐性遗传,小头畸形,眼球震颤,癫痫发作,全面发育迟缓,全身性肌张力减低,肌张力障碍,脑白质营养不良,婴儿期发病,出生后小头畸形,弥漫性脑白质异常,重度智力残疾,严重的全脑发育迟缓
4.精子形成障碍66型

精子形成障碍66型(Spermatogenicfailure66):精子形成障碍66型的特征是男性不育,因为所有精子都是圆头的(球形精子)且顶体缺失。临床表现:常染色体隐性遗传,男性不育,青年发病,圆头精子症。
5.Werner综合征

Werner综合征(Wernersyndrome):Werner综合征,又称成人早衰症,是一种罕见的常染色体隐性遗传病。平均发病时间是24岁,最早发病为6岁,死亡年龄中位数为47-48岁,平均死亡年龄54岁。
主要的几个临床症状:毛发脱落、白内障、萎缩或紧绷的皮肤、须发早白、软组织钙化、锐利的面部特征、声音异常高亢、身材矮小、生育能力低下。目前无治愈方法,主要是针对并发症做治疗。最近有证据表明,SB203580可能对治疗有所帮助。在美国发病约为1:200,000,在日本较高,为1:40,000-1:20,000。
临床表现:常染色体隐性遗传,性腺功能减退症,凸鼻嵴,白内障,视网膜变性,糖尿病,骨质疏松,毛发异常,骨肉瘤,脑膜瘤,身材矮小,早发性动脉粥样硬化,早衰面容,皮下钙化,硬皮病。
6.原发性纤毛运动障碍37型和精子生成障碍18型

原发性纤毛运动障碍是由纤毛结构缺陷导致的一种疾病,属常染色体隐性遗传病。可导致患者慢性支气管炎、支气管扩张、哮喘、慢性鼻炎、鼻窦炎、慢性中耳炎等。女性患者输卵管纤毛结构异常表现为生育力下降。男性精子尾部的鞭毛是一种特殊的纤毛,当其结构异常时,精子运动功能障碍,造成男性不育。部分患者由于胚胎期纤毛结构异常,缺乏正常的纤毛摆动,可出现左右身体不对称和内脏转位,形成kartagener综合征。
DNAH1基因变异引起的SPGF被称为18型SPGF。男性患者的精子鞭毛通常发生形态学异常,可能出现精子尾部缺失、过短、弯曲盘绕或宽度不均匀,导致精子运动能力完全丧失或大幅下降,临床上表现为少弱畸形精子症,造成男性不育。DNAH1基因变异是MMAF最常见的遗传因素,可解释29%~57%的患者。
根据相关文献报道,DNAH1基因突变的患者通过卵胞浆内单精子显微注射技术(Intracytoplasmic sperm injection,ICSI)辅助生殖预后良好。
本文是李建辉版权所有,未经授权请勿转载。 本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅
发表于:2024-09-11