 三甲
三甲
对面相逢不识君——茎突综合征
有一类缺血性卒中,无论你在意与否,它就躲藏在一行行病历里,隐匿在一张张影像中。隐源性卒中,指在全面的血管、心脏和血清学评估后(见附表),仍不能明确归因于心源性栓塞型、大动脉粥样硬化型或小动脉闭塞型的缺血性卒中。即缺血性脑卒中TOAST分型的不明原因型脑卒中。
从定义,我们可以推测隐源性卒中在所有缺血性卒中的比例,可能会随着临床医生对疾病认识的加深,以及影像、检验手段的更新而越来越低。我们今天带来的特殊病例,引起卒中的幕后黑手是大家熟悉而又陌生的颞骨茎突。
兴风作浪
患者男性,48岁,主因“言语不清伴左侧肢体麻木2个月”来诊。无咽部疼痛、异物感,无声音嘶哑、吞咽困难等。既往糖尿病、高脂血症病史。入院查体未见明显异常。
患者2个月前无明显诱因突发头晕、言语不清及左侧肢体麻木,当地医院行头颅MR提示右侧额顶枕叶点状新发梗塞灶。
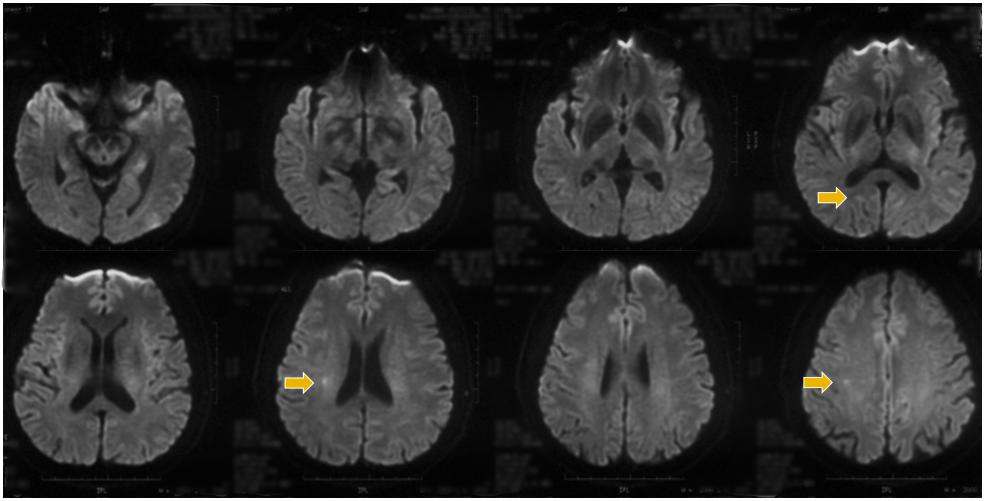
图1. 头部MR-DWI(发病3日)
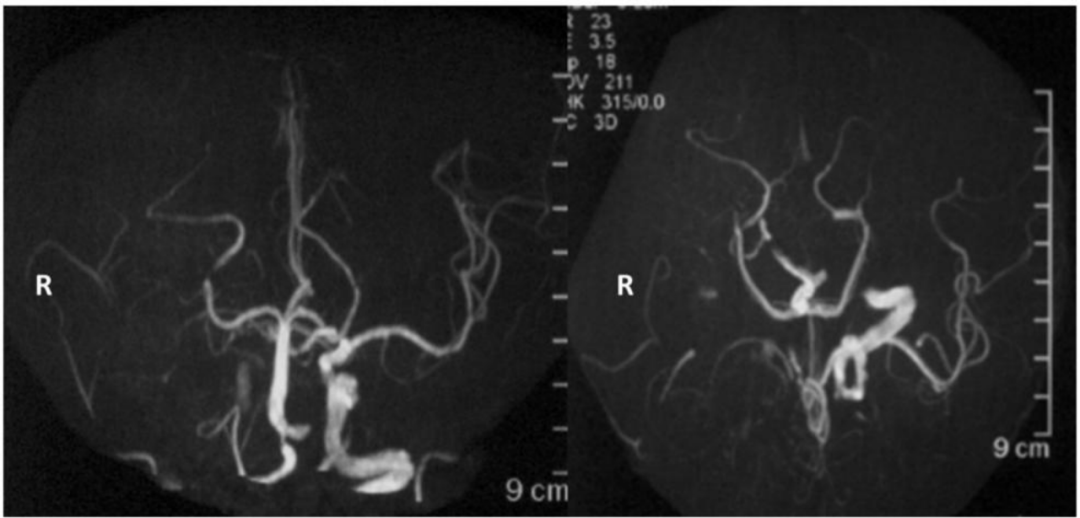
图2. MRA提示右侧颈内动脉闭塞(发病3日后)
头颈CTA(行MRA后4天),可见右侧颈内动脉显影。
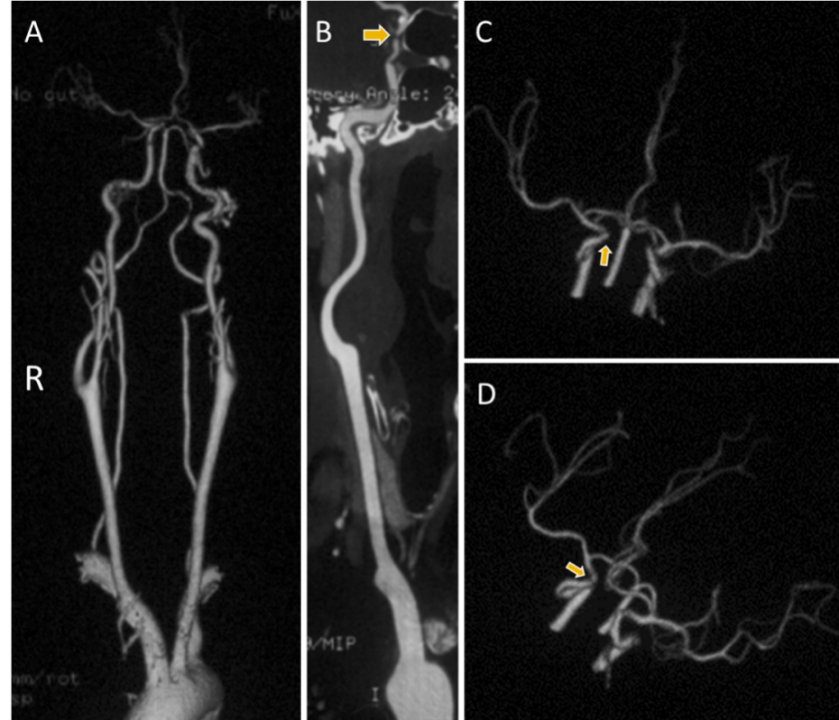
图3. 头颈CTA,示右侧颈内动脉C7段重度狭窄(B、C、D图箭头)
面对“失而复得”的右侧ICA,当地医院没有给出合理解释,给予常规的输液治疗,口服阿司匹林和阿托伐他汀,后就诊于其他医院仍未查到病因。这似乎是个熟悉的剧本。
事出反常
4天之内,右侧ICA闭塞再通,原因是什么?
我们需要逐一排除ICA闭塞再通的常见机制:
1. 不稳定性粥样硬化斑块破裂后闭塞再通;2. 急性斑块内出血导致闭塞,吸收后闭塞再通;3. 颈动脉夹层;4. 新生滋养血管;5. 血管痉挛。
其中第1-3点,在颈动脉超声及高分辨核磁中并未发现证据,可以排除。第4点是慢性闭塞再通的机制,病程较长,而且从血管形态看也不符合。于是我们把注意力聚焦到血管痉挛。
之前的宣武星期五《“又双叒叕”闭塞了——可逆性颈动脉闭塞》分析了一例复杂病例,临床诊断为可逆性血管收缩综合征(Reversible Cerebral Vasoconstriction Syndrome, RCVS),分析结果是茎突惹的祸,本例与之有相似之处。本例RCVS的诊断依据:1. 中年男性;2. 局灶性神经功能缺损;3. 血管影像可逆性表现(图3中C7段的“重度狭窄”,在两月后的造影中(图6)也消失了)。
RCVS的病因包括:使用血管活性药物、运动劳累、头部创伤及术后、蛛网膜下腔出血、颈动脉或椎动脉夹层、颈动脉壁受机械应力刺激等。在后续的CTA重建中,我们发现患者的右侧茎突过长,也许是茎突对颈动脉造成了刺激。有没有方法能验证呢?带着疑惑,我们联系到血管超声的同事,行颈动脉超声时加做转颈试验,结果如下:

图4. 我院颈动脉超声提示:头后仰位时,右侧大脑中动脉血流速度较基础血流下降38%
果然,我们发现了蛛丝马迹,患者头后仰时,右侧大脑中动脉血流速度较基础值下降38%,从侧面说明右侧茎突及其附属组织对同侧ICA的管壁造成了压迫。这又引出了新的问题:
为何患者头部后仰时导致同侧大脑中动脉血流速度下降,而不是常见的前屈位?
文献报道中,头前屈导致的血流障碍,多为茎突自身对颈内动脉管壁产生的直接压迫所致。而本例可能是茎突对其附属结构(肌肉、韧带)的牵拉和位移影响了颈内动脉的血流。无独有偶,Chopra等报道的病例中,一位29岁的年轻男性几年间数次在头部后仰时出现短暂晕厥,头位回正后即恢复正常。完善CTA发现一侧茎突过长,考虑与茎突及附属结构所致颈内动脉血流受限相关。
真相似乎浮出水面,我们的推测又能否解释患者发病及2个月后两次MR梗塞区域的不同呢?
患者两次MR提示的栓塞性质及原因分别是什么?
患者既往无房颤等心脏病史,入院心电图及心脏超声正常,暂排除心源性栓塞机制。
首次MR(图1)提示右额顶枕叶皮层点状新发梗塞。患者的前交通动脉开放,在右侧颈内动脉闭塞时,左侧颈内动脉血流向右侧代偿,弥补了部分右侧血流受限的影响,未形成大的前循环供血区梗塞灶。而点状梗塞灶考虑为动脉-动脉栓塞机制,颈内动脉闭塞引起管腔内血栓形成,血栓脱落导致栓塞发生。
第二次MR(图5)所示梗塞灶更靠近右侧半卵圆中心及内侧分水岭区域,考虑机制为血流动力学障碍,可能与头部活动导致茎突压迫ICA有关。
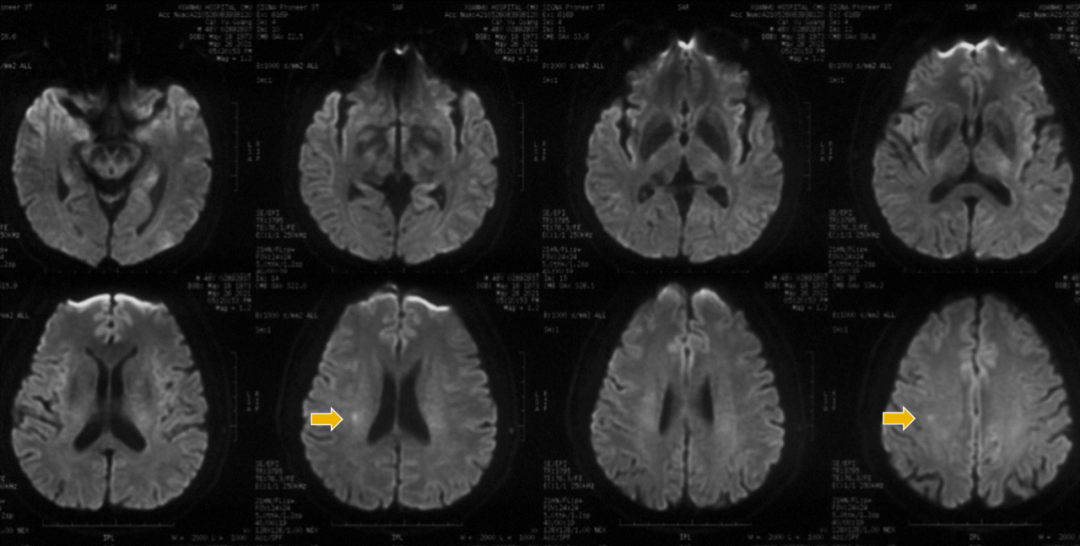
图5. 入院后(发病后2个月)MR提示右额顶新发梗塞灶
浮出水面
患者入院后完善各项血管检查,行DSA发现右侧ICA各段管径正常,前述CTA所示的C7段狭窄不复存在(图6)。左侧ICA C4段中度狭窄(图7)。

图6. 右侧ICA颅外及颅内部分DSA正侧位,可见右侧ICA管腔通畅
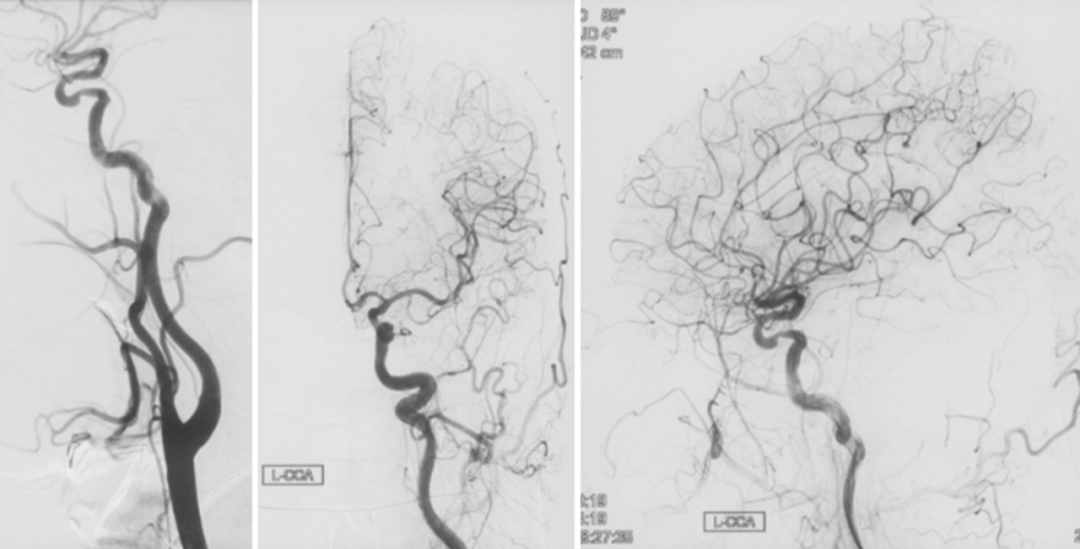
图7. DSA示左侧ICA C4段中度狭窄
仔细观察头颈CTA,我们可以看到造成上述问题的始作俑者——茎突(图8)。在高分辨核磁上,我们也可以寻到一些端倪(图11)。
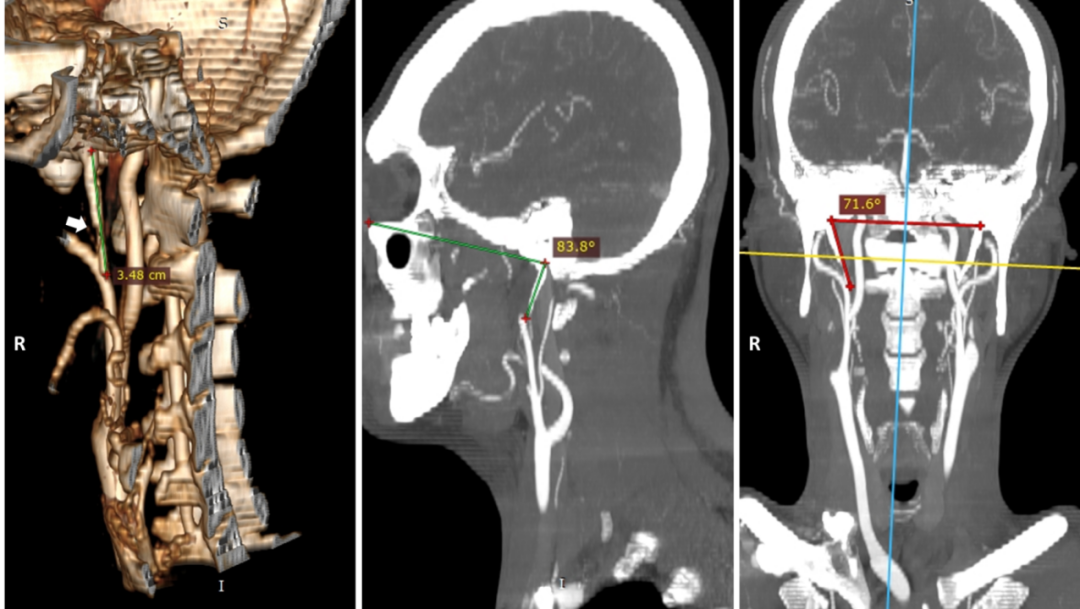
图8. 头颈CTA三维重建示右侧茎突长度为3.48cm,前倾角83.8°,内收角71.6°,茎突整体于颈内动脉前方向前下斜行。左图箭头所指处骨质结构不连续。
Tips: 标准茎突形态
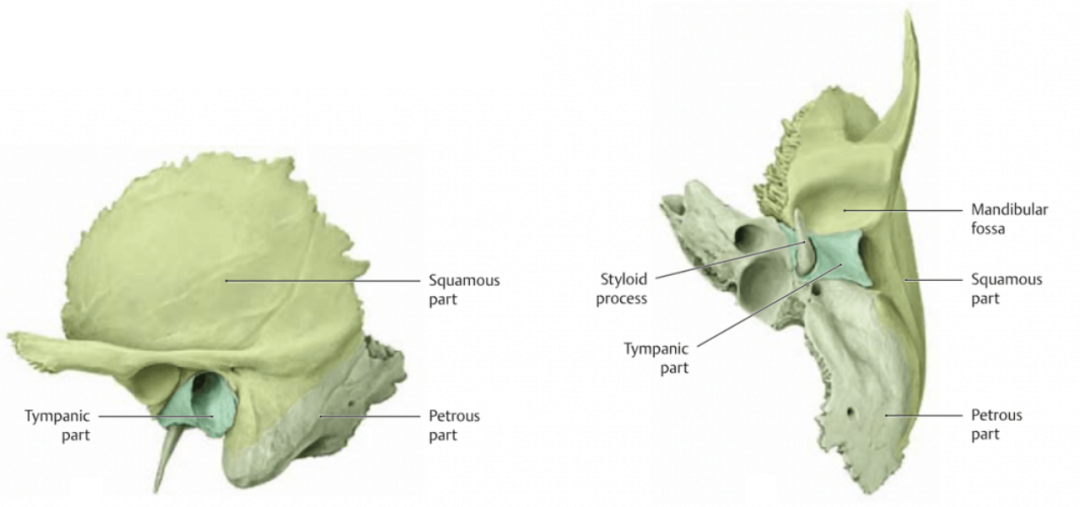
图9. 茎突位于颞骨鼓室部,起于茎乳孔前内侧,呈细长圆锥状,向内、前、下延伸,靠近下颌骨内侧。
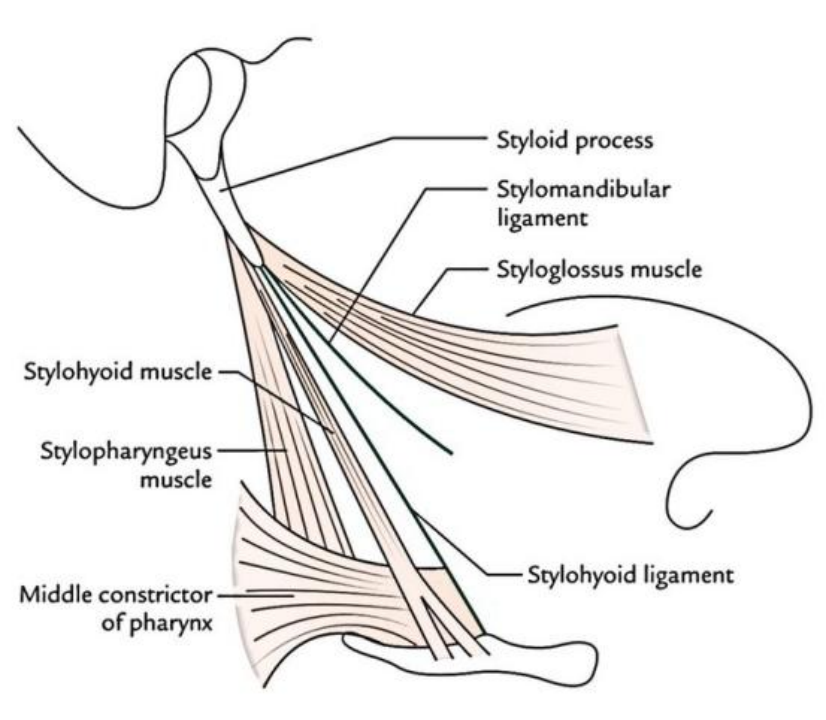
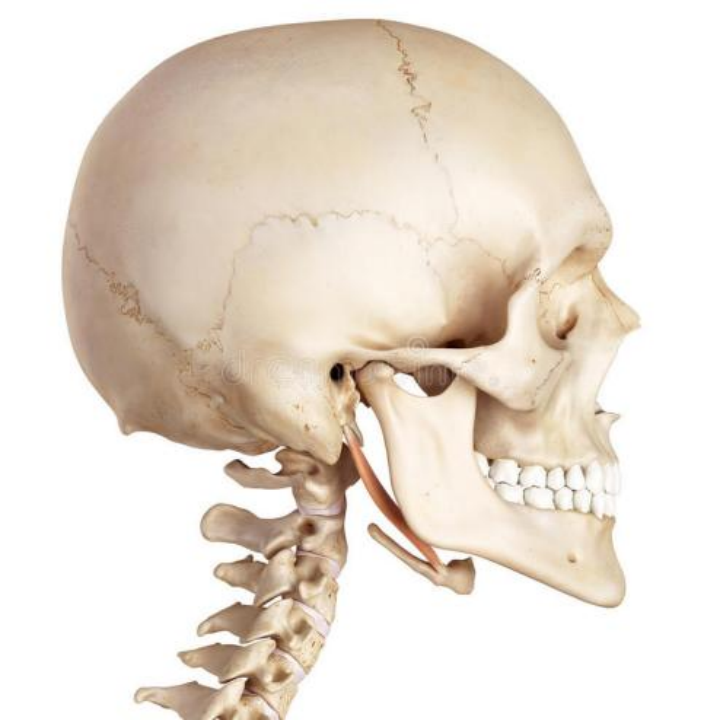
图10. 其中茎突舌骨韧带的骨化较常见,在一些病例中,难以区分茎突本身和已经骨化的茎突舌骨韧带。
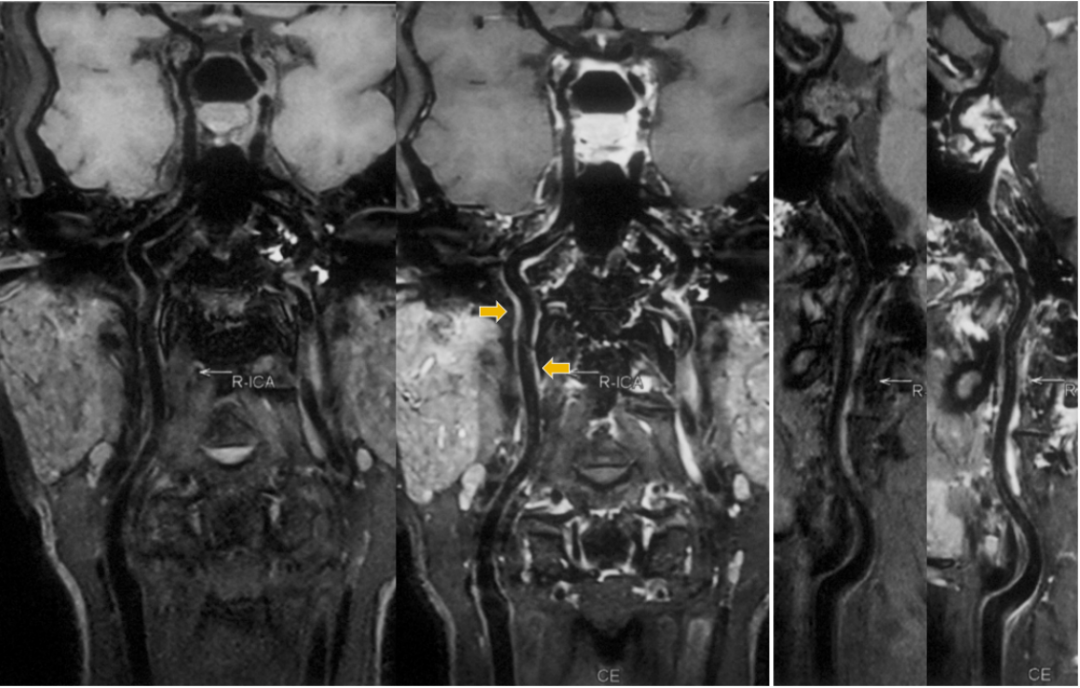
图11. 高分辨核磁的增强扫描提示右侧颈内动脉颅外段管壁增厚,略有强化(箭头所示),不排除为茎突刺激管壁导致的局部炎症。
就地正法
至此整个脉络就清晰了,确定诊断为右侧茎突综合征。具备手术指征:1. 典型的脑缺血症状;2. 影像学判断茎突长度、方位异常;3. 影像学判断头部活动引起茎突位移,导致脑血流速度明显改变。
我们采取经颈外入路茎突截短术,分离颈阔肌和胸锁乳突肌后,沿胸锁乳突肌颈外动脉分支及二腹肌间隙向深部找到茎突,于离茎突尖端2.0cm处离断(图12),剥离茎突骨膜,仔细分离茎突远端甲状舌骨韧带,切断长约2.0cm的茎突。
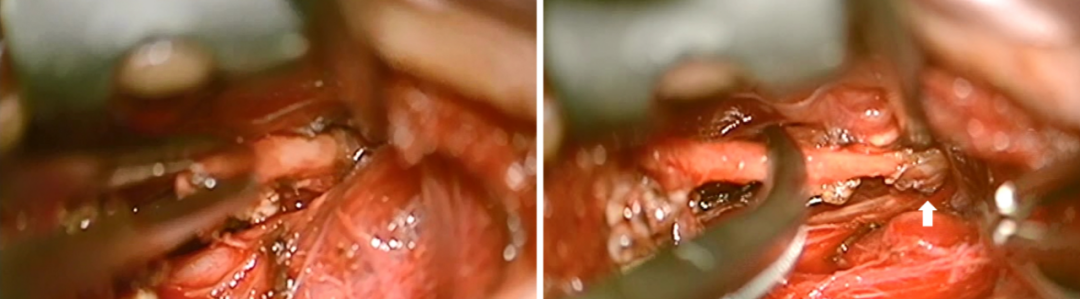
图12. 术中离断茎突。茎突从右图白色箭头所指处离断,此处为软组织连接而非骨质结构。
治疗茎突过长主要采取茎突截短术,分为经口咽入路及经颈外入路。
耳鼻喉科及口腔科医生更擅长经口咽入路,优点为体表无切口,无可见疤痕;缺点:1. 术野狭小,对深部神经血管显露不充分,存在损伤风险;2. 属于Ⅱ类切口,增加术后感染几率;3. 切口可能瘢痕愈合,遗留咽部异物感。
神经外科及头颈外科医生更青睐经颈外入路,优点为术野显露充分;缺点:1. 形成体表瘢痕;2. 创伤较大,存在面神经损伤的风险。
术中还有一处细节,茎突离断处并不是骨质结构,而是类似韧带的软组织,问题来了:术中离断茎突处与CTA上茎突骨质的不连续部位是否一致?
对比术前和术后CTA,结合术中所见,考虑软组织处与影像上茎突骨质不连续的位置一致。Langlais等总结了茎突过长的三种形态:1. 延长型;2. 假关节型;3. 节段型(图13)。Gossman和Tarsitano的研究中,节段型占所有茎突过长总数的27%,解剖时发现段与段之间的软组织由肌纤维或软骨成分构成。本例患者的茎突属于节段型。不同分型与茎突过长形成的机制有关,目前具体成因尚不明确,包括先天机制、成骨机制、外伤或炎症刺激机制、茎突附属物钙化机制等学说。
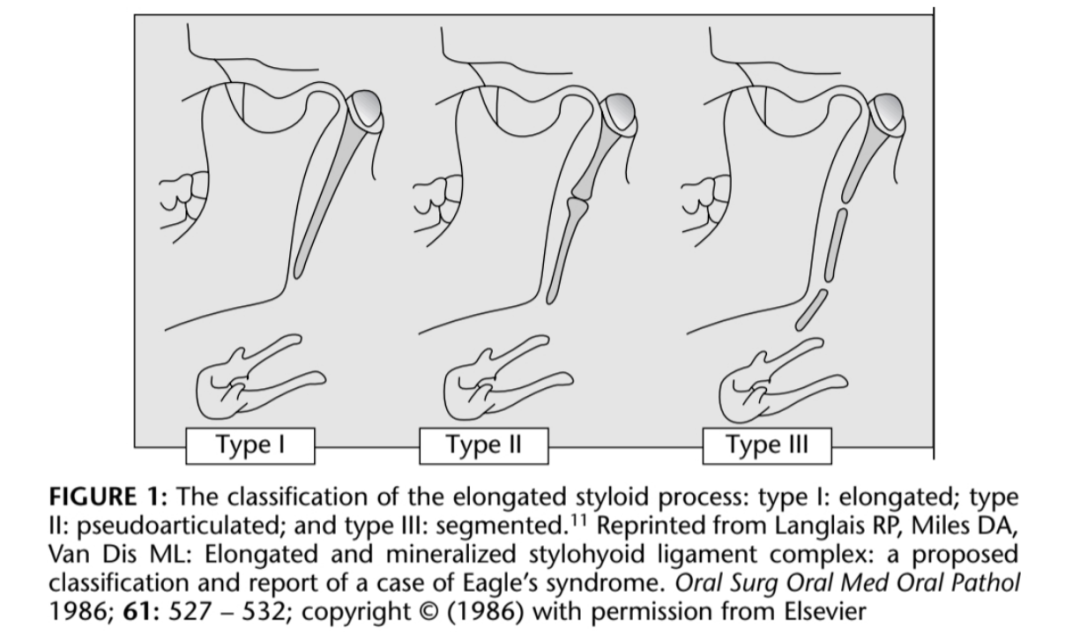
图13. 茎突过长的分型
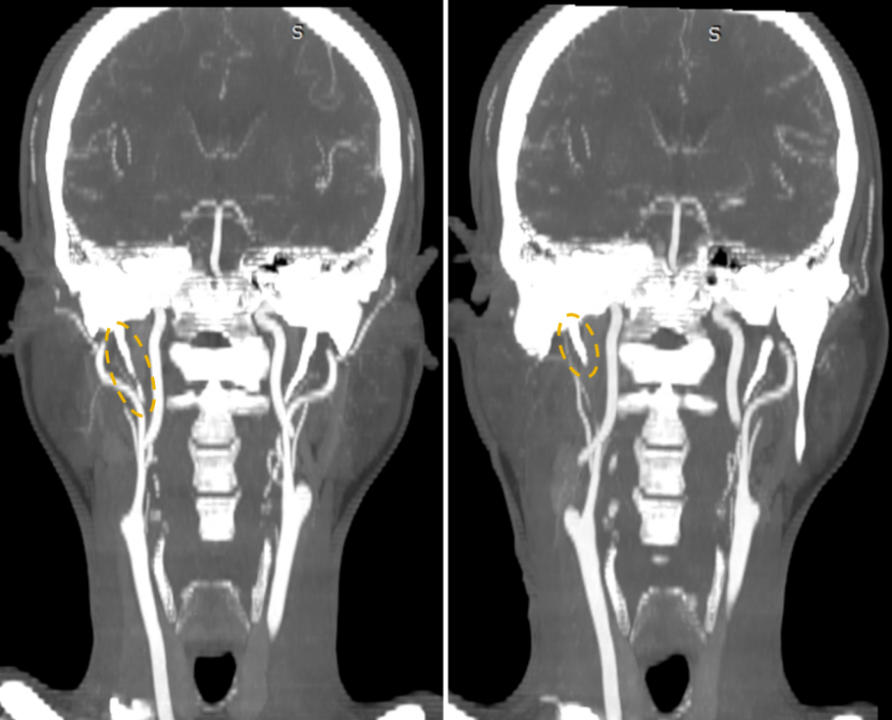
图14. 术前(左图)与术后(右图)右侧茎突长度的对比
患者术后行口服单抗及他汀治疗,术后半年复查颈动脉超声,头部后仰时未见右侧大脑中动脉血流下降。术后2年随访,患者未再出现言语不清及左侧肢体麻木症状。
茎突过长的历史由来:
1651年
意大利帕多瓦大学的解剖学家Pietro Marchetti在解剖时发现茎突至舌骨的骨化。

图15. Pietro Marchetti (1589-1673)
1872年
Wein Lecher成为首位切断茎突以解除患者症状的医师。
1937年
杜克大学的耳鼻喉科医生Watt Eagle首次描述由茎突过长诱发的“stylagia”,并于此后陆续发表茎突异常的报道,此病以他的名字命名为Eagle syndrome。

图16. Watt W. Eagle (1898-1980)
Eagle syndrome的经典症状:口咽及颈面部疼痛、咽部异物感、吞咽困难,头部转动时症状可能加重。有关研究的先驱以耳鼻喉科医生为主,而Watt Eagle首先归纳出Eagle syndrome的脑血管相关症状:晕厥、黑矇、失语、肢体麻木无力等,为神经内外科医生认识Eagle syndrome打开了大门。
流行病学:
- 茎突过长的人群发生率为4%-7%,其中10%为症状性;
- 发病年龄50岁左右;
- 男:女=16:3;
- 左右两侧的发病率无明显差别;
- 常累及双侧,但少有双侧同时出症状。
我们患者的问题虽然解决了,却暴露出更大的隐忧:1. 如果脑血管病医生对茎突过长不了解,即便患者完善了头颈CTA,医生可能只关注血管情况,而忽视茎突的异常;2. 如果未考虑到茎突过长,和血管超声团队未事先沟通,在行颈动脉超声时,超声医师大概率不会对患者行转颈试验,又会失去一个重要的诊断依据。
本例患者,若找不到根本病因,被“可逆性颈动脉闭塞”虚晃一枪而进行药物保守治疗,患者可能还在因为卒中复发而辗转各家医院,甚至出现不可挽回的缺血事件。似乎所有关于缺血性卒中的悬案,都可归类于隐源性卒中,但确立“隐源性卒中”这一诊断之前,需慎之又慎。
多项大型流行病学研究报道,隐源性卒中占缺血性脑卒中的25%-40%。牛津大学对4项大型人群研究进行的meta分析显示,隐源性卒中患者在发病后7天、1个月及3个月时,卒中复发的风险分别为1.6%、4.2%和5.6%。2年的卒中复发风险达到14%-20%。由此可见,明确隐源性卒中的病因并及时治疗非常重要。
近几年,颈动脉蹼作为隐源性卒中的重要组成部分,逐渐被临床医生了解,医生们愿意更仔细地判读和甄别CTA上颈动脉球部的特殊影像,越来越多的漏网之蹼被识破。目前关于茎突过长和缺血性卒中关系的研究还多集中于个案和小样本的回顾性分析,尚不明确其在隐源性卒中内所占比重。但考虑到茎突过长并不低的人群发生率(4%-7%),其中发生茎突综合征的比例达到10%(包括缺血及非缺血症状),是时候把它从隐秘的角落里揪出来了。
总结
本例患者的右侧茎突长度为3.48cm,和本中心以往类似患者相比,其长度并不算突出,仍导致了同侧前循环的血流动力学障碍。值得思考的是,茎突的长度只是评价茎突形态、位置的其中一项指标,此外还包括茎突的薄厚、内收角、前倾角、以及其附属组织的钙化程度等。
所以对于特定患者,建议综合测量茎突相关指标,评判其与颈动脉的位置关系,并进行不同头位下的颈动脉超声检查以明确诊断。更重要的是,目前国内缺乏如颅外段颈内动脉狭窄等疾病与茎突形态学关系的研究,尽早拿出中国数据,重视对茎突综合征的诊断与治疗,势在必行。
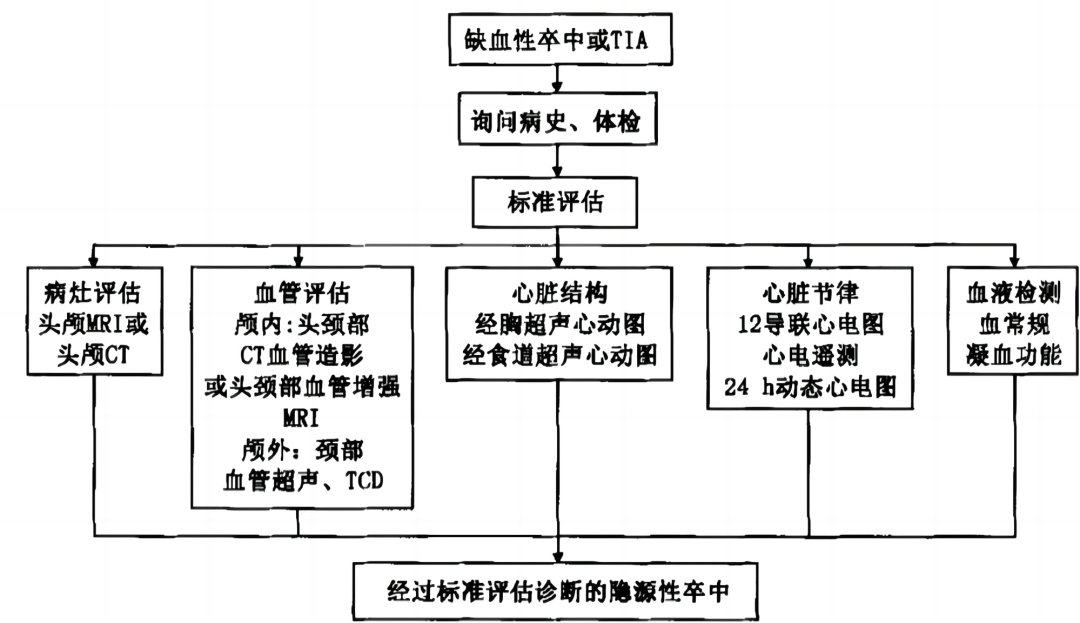
附表:隐源性卒中的评估流程

作者:许文龙
首都医科大学宣武医院
主治医师,医学博士,毕业于中国医科大学,2016年到宣武医院神经外科工作至今。主要工作方向为颈动脉狭窄、椎动脉狭窄、颅内动脉狭窄、烟雾病等缺血性脑血管病的外科及介入治疗。

作者:陈飞
首都医科大学宣武医院
神经内科主治医师,医学博士,毕业于第三军医大学,并在陆军总医院完成博士后研究,先后师从于帅杰教授和张微微教授,目前作为脑血运重建中心的神经内科医生,接受严格的神经介入培训。

作者:王亚冰
首都医科大学宣武医院
博士学位,师从于凌锋教授,曾留学法国,现任首都医科大学宣武医院神经外科副主任医师,缺血专业组主诊组长,对于缺血性脑血管病而言,是手术和介入治疗的双面专家,每年在宣武医院完成各类手术和介入治疗超过400例。作为骨干参与国家科技部十二五、十三五研究,主持完成了国内颅内动脉狭窄介入治疗的多中心大样本队列研究—CRTICAS,先后发表10余篇SCI文章,其中,2018年完成药物涂层球囊治疗椎动脉狭窄的国际首例报道,发表在权威的JACC杂志。
本文是陈飞版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论