 三甲
三甲
免疫球蛋白临床应用的适应症和相对禁忌症及副作用
文章摘要:免疫球蛋白是一种由人类血浆制成的抗体,广泛应用于治疗免疫缺陷和自身免疫疾病等领域。本文介绍了免疫球蛋白的历史、应用和使用证据。
(一)概述
免疫系统拥有一套高度先进和协调的机制,允许生命体区分“自我”和“非自我”。 宿主可以同时利用先天和适应性免疫应答机制来识别和清除病原微生物。免疫球蛋白是由分化自B淋巴细胞的浆细胞产生的抗体, 人免疫球蛋白是临床上应用最广泛的血液制品。 免疫球蛋白制剂是由数千名健康捐赠者汇集的人类血浆制成的,这使得免疫球蛋白制剂含有大量和不同的抗体库。由于依赖捐赠的血浆,因此免疫球蛋白供应是十分有限的。对免疫球蛋白治疗的需求每年以6-8%的速度增长,继发性免疫缺陷对免疫球蛋白需求增长尤为明显。 全球血浆采集存在严重的不平衡,其中65%来自美国。
虽然 部分患者适当的注射免疫球蛋白可以挽救生命,但临床医生必须熟悉如何管理与免疫球蛋白输注相关的各种不良事件。 开具免疫球蛋白处方的临床医生需要更好地认识免疫球蛋白治疗的当前临床适应症和支持其用于免疫紊乱的证据水平。
在过去的30年里,关于富含IgM的静脉注射免疫球蛋白治疗脓毒症的益处,已经发表了大量的文献,存在相互矛盾的结论; 因此,免疫球蛋白治疗脓毒症仍然是一个有争议的话题。 由于缺乏高质量的证据,目前最新版的《拯救脓毒症行动指南》并不推荐在脓毒症患者中使用静脉注射免疫球蛋白。
目前公认的免疫球蛋白适应症有:原发性免疫缺陷、继发性免疫缺陷(多发性骨髓瘤或慢性淋巴白血病)、川崎综合征、免疫性血小板减少性症、格林巴利综合征、骨髓移植后移植物抗宿主病和儿童HIV相关性持续感染。
免疫球蛋白应用相对禁忌症:1、对免疫球蛋白过敏或者有其它严重过敏史的患者。2、选择性IgA缺乏且具有IgA抗体患者(有选择性IgA缺乏症的病人接触血浆IgA或丙种球蛋白后,会产生抗IgA抗体,以后如再输血或接触免疫球便引起严重过敏反应)。3、发热患者慎用。
静脉注射免疫球蛋白血栓发生情况:据估计每个疗程的血栓发生率为0.15-1.2%。但2003年报告病例的大幅增加表明,真实发病率可能明显更高。 动脉血栓形成在IVIG治疗后早期发生(49%在4 h内,77%在24 h内),并与高龄和动脉粥样硬化性血管疾病有关; 静脉血栓形成发生较晚(54%在给予IVIG后24小时以上),并与导致静脉淤滞的因素(肥胖和行动不便)有关。
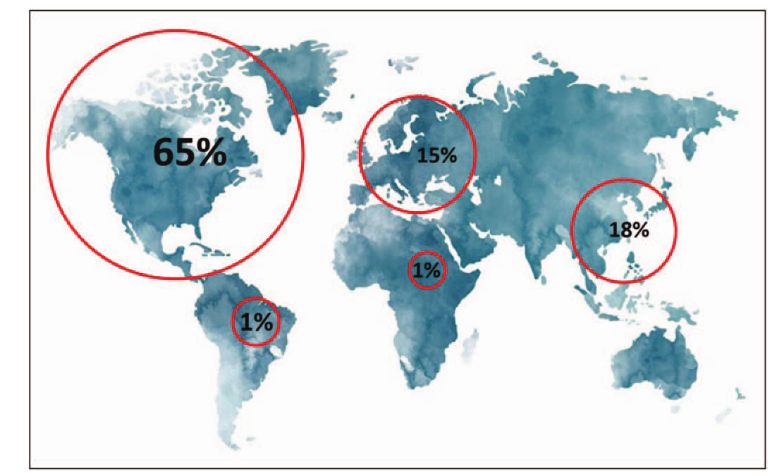
血浆(来源和回收)收集的全球分布(基于市场研究局的数据)
(二)免疫球蛋白使用历史
用抗体治疗疾病的历史始于19世纪,破伤风和白喉毒素被发现后,人们认识到这些生物引起的感染,促使人体产生的免疫力可以通过免疫血清转移。 人类免疫球蛋白(IG)是在第二次世界大战(1941-1945年)早期发展起来的,当时由EJ Cohn和JL Oncley领导的一个小组使用酒精分级人类血浆来开发用于战争伤员失血的浓缩白蛋白和用于预防感染的丙种球蛋白。1952年,Bruton首次使用IG治疗第一例确诊为无丙种球蛋白血症的患者。
然而,由于早期免疫球蛋白产品纯度低,静脉注射(IV)给麻疹儿童导致严重的不良反应(AEs),包括抽搐、发热、坐立不安、寒战,甚至循环衰竭。安全输注更大剂量免疫球蛋白的愿望导致了生产工艺的改进,这种进步也使得炎症和自身免疫疾病成为了免疫球蛋白的另一个应用的主战场。更浓缩的免疫球蛋白制剂的出现,使得以家庭为基础的皮下注射成为可能。Berger等人在1980年首次使用皮下输注免疫球蛋白(SCIG)治疗抗体缺乏。
(三)免疫球蛋白在治疗中的地位和使用证据
1. 原发性免疫缺陷疾病
原发性免疫缺陷疾病是一组高度异质性的影响先天和适应性免疫系统中不同组分的遗传性疾病。这些组分可能是巨噬细胞、自然杀伤细胞、树突状细胞、中性粒细胞、补体蛋白、B淋巴细胞和T淋巴细胞等。原发性免疫缺陷相对少见,可能单独发生或作为综合征的一部分发生。 原发性免疫缺陷往往在婴儿期或儿童期变得明显,但许多原发性免疫缺陷存在于成年期,估计原发性免疫缺陷的总发病率为每1200人中有1人。
(1)无丙种球蛋白血症(Agammaglobulinemia):对无丙种球蛋白血症患儿的历史回顾性资料表明,与感染相关的并发症的数量和严重程度与静脉注射免疫球蛋白(IVIG)剂量呈负相关。事实上,当免疫球蛋白G的最低值保持在500mg/dL以上时,严重的细菌性疾病就可以预防。Orange等荟萃分析结果表明, IgG最低水平每升高100 mg/dl,肺炎发病率下降27%。 最低水平为1000 mg/dl的患者的肺炎风险是最低水平为500 mg/dl的患者的五分之一。 结论:较高的谷期IgG水平可以逐渐降低无丙种球蛋白血症肺炎风险。
(2)低丙球蛋白血症(Hypogammaglobulinemia):免疫球蛋白替代适用于反复细菌感染和血清Ig水平降低的患者,这些患者对蛋白质或多糖疫苗攻击也没有反应。 例如,患者可能无法产生针对破伤风类毒素和/或肺炎球菌多糖疫苗的IgG抗体。
(3)特异性抗体缺乏症(Specific Antibody Deficiency):如果已经确定了严重的多糖无反应(针对23价肺炎球菌多糖疫苗),并且有证据表明复发性细菌感染需要进行抗生素治疗的患者应接受免疫球蛋白替代治疗
(4)免疫机制不明导致的反复感染(Recurrent Infections Due to Unknown Immune Mechanism):一致认为,在这些疾病的免疫球蛋白治疗是一个有用的辅助治疗。 数据表明,一些患有高IgE综合征和反复呼吸道感染的患者从免疫球蛋白替代中受益。在一项对73个中心和507名患者的研究中,支持在WAS(Wiskott-Aldrich syndrome)患者中使用预防性抗生素替代免疫球蛋白。估计12%至15%的共济失调毛细血管扩张(AT)患者需要免疫球蛋白治疗
2.继发性免疫缺陷
免疫球蛋白替代疗法已用于多种导致继发性体液缺乏的疾病,包括恶性血液病、儿科艾滋病毒感染、早产、老年疾病、实体器官或骨髓移植相关的低丙种球蛋白血症,以及接受B细胞耗竭药物治疗的患者
(1) 慢性淋巴细胞白血病(CLL) :复发性感染在CLL患者中造成大量的发病率和死亡率,导致30%-50%的死亡。低丙种球蛋白血症是CLL的常见并发症,来自CLL患者的研究数据证明了免疫球蛋白替代治疗对预防感染的好处。 Raanani等评估了CLL和多发性骨髓瘤患者的多项试验,发现在免疫球蛋白治疗的患者中,主要感染的发生显著减少(相对风险,0.45)。 尽管在这项试验中没有发现生存益处,但研究人员得出结论,对于CLL和低丙种球蛋白血症患者,应该根据个体情况考虑免疫球蛋白替代治疗。临床医生可能会考虑对CLL和复发性严重细菌感染的患者进行替代免疫球蛋白治疗,这些患者在接受白喉、破伤风或肺炎球菌疫苗后抗体水平低于保护水平。必须要强调的是,患者选择免疫球蛋白治疗应基于经证实的抗体产生缺陷,而不是仅基于低丙种球蛋白血症。事实上, 目前的治疗指南明确指出,低丙种球蛋白血症本身并不构成启动CLL治疗的基础。
(2) 多发性骨髓瘤:感染是MM患者发病率和死亡率增加的主要因素。来自MM患者研究的数据已经证明了免疫球蛋白替代治疗对预防感染的好处。 多项试验的结果表明,免疫球蛋白治疗的MM患者的主要感染发生率显著下降。最近对47例有复发性中重度细菌感染史的MM患者的分析表明,静脉注射免疫球蛋白治疗后感染率显著下降。 36对于MM患者、低丙种球蛋白血症和已证实的抗体缺陷患者,应根据个人情况考虑免疫球蛋白替代治疗。3.在严重感染患者中,免疫球蛋白替代治疗率从17%降至0%,中度感染患者从55%降至34%,轻度感染患者从28%降至21%。
3. 自身免疫性疾病
(1)格林-巴利综合征(GBS)是一种脱髓鞘性周围神经病变,这种疾病被认为是由周围神经系统髓鞘或雪旺细胞的免疫破坏引起的,是一种感染后发生的综合征,最常见的是空肠弯曲菌,尽管EB病毒、肺炎支原体和流感病毒也与GBS的发展有关。 快速和进行性虚弱是GBS的一个关键特征,通常在4周内达到,随后是持续数周至数月的平台期。GBS可结合静脉注射免疫球蛋白、皮质类固醇和血浆置换进行治疗。静脉注射免疫球蛋白通常为0.4g/kg剂量连续5天。
(2)川崎病(Kawasaki disease,KD)又称粘膜皮肤淋巴结综合征,发生于儿童。 它的特点是发烧、皮疹、手足肿胀、眼睛发红和发炎、口腔和喉咙发炎以及颈部淋巴结肿大。在急性期给予静脉注射免疫球蛋白和阿司匹林被认为是儿童KD的标准护理,以防止心脏并发症,特别是冠状动脉瘤的发展。标准的KD一线治疗中心是在病情明显时的前10天内,推荐剂量为2g/kg的静脉注射免疫球蛋白和80mg/kg至100mg/kg的口服阿司匹林。 该方案在预防冠状动脉瘤发展方面显示出显著的疗效。 然而,大约15%-20%的患者接受这种方案治疗将需要二次静脉注射免疫球蛋白治疗来控制炎症。
(3)免疫性血小板减少症(ITP),皮质类固醇是ITP治疗的基石。 静脉注射免疫球蛋白也被推荐用于一线治疗。 静脉注射免疫球蛋白能迅速增加血小板计数,是那些活动性出血患者的首选治疗方法。
(4)慢性炎性脱髓鞘性多发性神经病 (CIDP) 表现为手臂和腿部进行性虚弱,并伴有四肢感觉功能受损。这种疾病与GBS密切相关。在过去的20年里,免疫球蛋白与皮质类固醇和血浆置换一起成为CIDP治疗方案的一部分。 117例接受静脉注射免疫球蛋白或安慰剂的CIDP患者, 结果显示,54%接受静脉注射免疫球蛋白治疗的患者调整后的残疾评分有所改善,而接受安慰剂治疗的患者为21%。
总之, 免疫球蛋白治疗是许多免疫性和炎症性疾病的基本和标准,也被确定用于其他疾病,而不仅仅限于本文讨论的疾病。适当使用免疫球蛋白可以降低疾病发病率,甚至挽救生命。 随着免疫球蛋白给药适应症的日益增多,医疗保健专业人员必须充分理解该疗法的最佳使用。 免疫球蛋白治疗需要应用于有充分研究证据支持的地方,以及它将提供最大临床益处的地方。
当然,是药三分毒,免疫球蛋白也不例外,由于IgG分子本身的抗原性、大分子量的IgG聚集、补体激活或单个核细胞直接释放细胞因子或存在对循环的微生物抗原或自身抗原的抗体等原因,输注免疫球蛋白可能会发生一些不良反应,发生概率大约5%到15%。 最常见的即时反应是发冷、发烧、头痛和肌肉疼痛。 大多可以通过口服预用药来消除或预防,如苯海拉明等抗组胺药和对乙酰氨基酚等非甾体抗炎药。 这些过敏反应的风险正在逐渐降低,从2009年的14.87%-10下降到2017年的4.39%-18,总体上很少,18岁以下的人过敏反应的相对风险增加。
参考文献:
Perez EE. Immunoglobulin use in immune deficiency and autoimmune disease states. Am J Manag Care. 2019 Jun;25(6 Suppl):S92-S97.
K B Megha,P V Mohanan. Role of immunoglobulin and antibodies in disease management. Int J Biol Macromol . 2021 Feb 1;169:28-38.
Martinez C, Wallenhorst C, van Nunen S. Intravenous immunoglobulin and the current risk of moderate and severe anaphylactic events, a cohort study. Clin Exp Immunol. 2021 Dec;206(3):384-394.
Prevot J, Jolles S. Global immunoglobulin supply: steaming towards the iceberg? Curr Opin Allergy Clin Immunol. 2020 Dec;20(6):557-564.
Kakoullis L, Pantzaris ND, Platanaki C, Lagadinou M, Papachristodoulou E, Velissaris D. The use of IgM-enriched immunoglobulin in adult patients with sepsis. J Crit Care. 2018 Oct;47:30-35.
Paran D, Herishanu Y, Elkayam O, Shopin L, Ben-Ami R. Venous and arterial thrombosis following administration of intravenous immunoglobulins. Blood Coagul Fibrinolysis. 2005 Jul;16(5):313-8.
本文是李登举版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论